各有關(guān)藥品生產(chǎn)企業(yè):
為做好2011年云南省醫(yī)療機構(gòu)藥品集中采購(非基本藥物部分)工作�,現(xiàn)對近期各生產(chǎn)企業(yè)關(guān)于采購公告及采購文件的咨詢問題進(jìn)行統(tǒng)一解答。
1. 關(guān)于申報賬號及密碼
1)云南省藥品耗材采購交易監(jiān)管平臺(http://www.ynyyzb.com.cn)左側(cè)藥品交易系統(tǒng)(藍(lán)色字體)申領(lǐng)申報賬號及密碼功能已關(guān)閉���。
未領(lǐng)取申報賬號及密碼的藥品生產(chǎn)企業(yè)��,按預(yù)公告規(guī)定攜帶企業(yè)法定代表人授權(quán)委托書原件(格式見預(yù)公告附件)��、營業(yè)執(zhí)照(副本)復(fù)印件(加蓋單位鮮章)在云南省藥品耗材采購交易監(jiān)管平臺(云南省昆明市人民西路205號3樓301室)進(jìn)行現(xiàn)場申領(lǐng)��。
申報密碼均由系統(tǒng)自動生成���,由字母(區(qū)分大小寫)及數(shù)字隨機組合。
企業(yè)名稱發(fā)生變更的藥品生產(chǎn)企業(yè),可先按上述規(guī)定申領(lǐng)密碼��,遞交紙質(zhì)申報材料時同時遞交企業(yè)相關(guān)變更證明(裝訂于其他證明(澄清)資料冊)���。
2)完成申報賬號及密碼領(lǐng)取工作后��,如由于密碼遺失或其他原因無法登錄藥品交易系統(tǒng)�,請按平臺首頁左下側(cè)操作幫助(藍(lán)色字體)企業(yè)賬號密碼管理相關(guān)規(guī)定辦理密碼初始化�。
2. 關(guān)于粘貼冊第二條第7.A.C)款中GMP證書說明
GMP證書:提供企業(yè)擬申報品種的GMP證書。GMP證書在換證期間的���,接收資料截止前提交省級以上藥監(jiān)部門出示的通過GMP現(xiàn)場檢查的證明文件的����,可以參與報價���。
3. 關(guān)于粘貼冊附表3投標(biāo)產(chǎn)品匯總表中“國家編碼”
國家編碼指:藥品本位碼�,可通過“國家食品藥品監(jiān)督管理局-數(shù)據(jù)查詢”(http://app1.sfda.gov.cn/datasearch/face3/dir.html)查詢�����。
4. 關(guān)于采購文件第三章第15條中“藥監(jiān)證明”���、粘貼冊第三條2)“藥監(jiān)證明”
藥監(jiān)證明指:企業(yè)所在地的省食品藥品監(jiān)督管理部門開具的二年內(nèi)無生產(chǎn)假藥及其他嚴(yán)重違反藥品監(jiān)督管理規(guī)定行為的證明原件����。
5. 關(guān)于粘貼冊第二條8.2)E物價文件復(fù)印件
政府定價藥品須提供國家發(fā)改委或云南省價格主管部門最新公布的藥品最高零售價有效證明文件復(fù)印件。如上述均無��,提供企業(yè)所在地價格主管部門最新公布的藥品最高零售價有效證明文件復(fù)印件����。
6. 關(guān)于包裝
同一生產(chǎn)企業(yè)���、同一通用名����、劑型����、規(guī)格下,可自行選擇一種包裝品種進(jìn)行申報�����,其余包裝品種可在藥品入圍后按有關(guān)規(guī)定進(jìn)行增補��。
7. 關(guān)于配送
企業(yè)維護(hù)企業(yè)后,可根據(jù)平臺配送企業(yè)目錄勾選配送企業(yè)����,不需遞交配送企業(yè)資料冊。如需委托平臺目錄以外的配送企業(yè)����,按粘貼冊要求遞交“配送企業(yè)資料冊”,經(jīng)審查合格后��,由平臺錄入系統(tǒng)配送企業(yè)目錄�����;此后��,企業(yè)方可進(jìn)行勾選����。
8. 關(guān)于裝盒
企業(yè)如無新增產(chǎn)品,不需提供新增產(chǎn)品檔案盒��;企業(yè)如不需申報第一��、二�����、三質(zhì)量層次,且無粉針劑亞劑型證明�,不需提供質(zhì)量層次證明資料冊及相應(yīng)檔案盒;企業(yè)如不需申報平臺配送企業(yè)目錄外的配送企業(yè)�,不需提供配送企業(yè)資料冊及相應(yīng)檔案盒
9. 關(guān)于收費
本次網(wǎng)上藥品集中采購不收取藥品生產(chǎn)企業(yè)任何費用。其他任何媒介或機構(gòu)或個人發(fā)布的收費信息均與本次網(wǎng)上藥品集中采購無關(guān)�,請各藥品生產(chǎn)企業(yè)注意。
10. 工作程序示意
后附���。
? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? 云南省藥品耗材采購交易監(jiān)管平臺
? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? ? 2010年11月9日
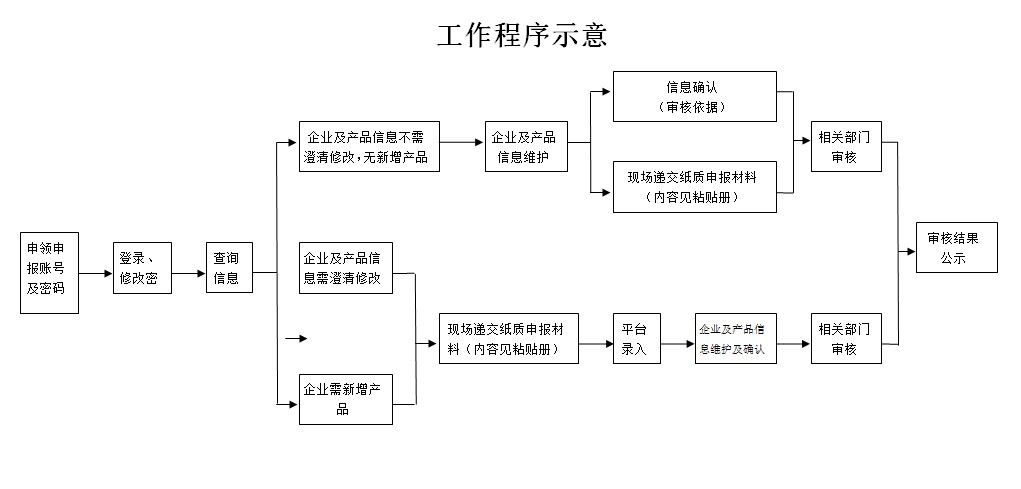
注:
1. 系統(tǒng)已有品種信息、需修改品種信息��、新增品種信息均須按照粘貼冊要求提交紙質(zhì)申報材料��。
2. 需修改品種信息����、新增品種信息相關(guān)紙質(zhì)申報材料,經(jīng)審核錄入后�����,方可進(jìn)行網(wǎng)上信息維護(hù)��,請各有關(guān)生產(chǎn)企業(yè)盡快遞交紙質(zhì)申報材料,并隨時關(guān)注藥品招標(biāo)系統(tǒng)內(nèi)信息變動�����。
3. 產(chǎn)品信息頁面所列信息為審核重要依據(jù)�,點擊確認(rèn)按鈕后,無法再進(jìn)行修改��,請慎重填寫�、提交。